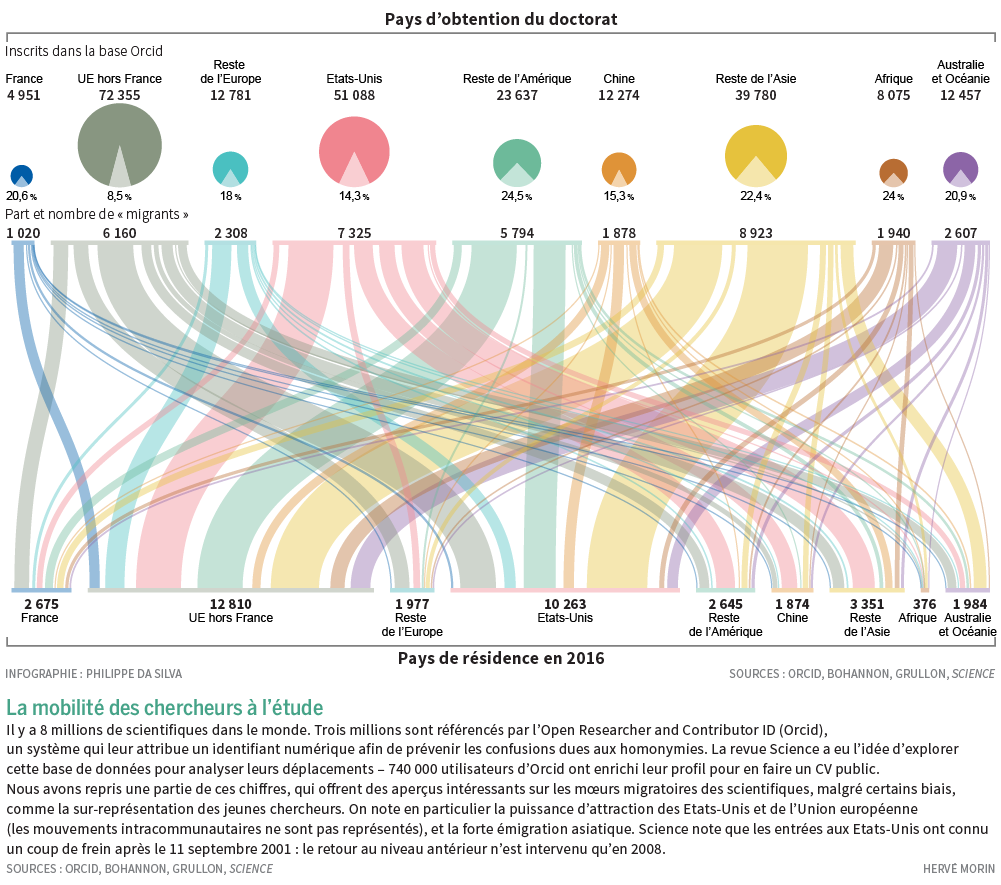
Voici une infographie tirée du Monde Science et Techno du 23/05/2017. Celle-ci a été permise grâce au numéro ORCID qui permet d’identifier, de façon non ambiguë tout chercheur contributeur d’une publication scientifique. Selon l’Open Researcher and Contributor ID, « ORCID est une organisation à but non lucratif qui a pour objectif d’aider à créer un monde dans lequel tous les intervenants dans les domaines de la recherche, de l’université et de l’innovation sont identifiés de manière unique et sont reliés à leurs contributions et à leurs affiliations, au-delà des limites des disciplines, des frontières et des époques. » Concernant les migrations de chercheurs, l’Union Européenne et les Etat-Unis restent attractifs. En France, un cinquième des chercheurs ayant obtenu leur diplôme sur le territoire, émigre, ce qui est plutôt beaucoup… une question peut se poser : est ce que la proportion de chercheurs quittant leur pays d’obtention de doctorat ne serait pas inversement proportionnelle à l’intérêt de ce pays pour sa propre recherche scientifique…?
Voici une infographie tirée du Monde Science et Techno du 23/05/2017. Celle-ci a été permise grâce au numéro ORCID qui permet d’identifier, de façon non ambiguë tout chercheur contributeur d’une publication scientifique. Selon l’Open Researcher and Contributor ID, « ORCID est une organisation à but non lucratif qui a pour objectif d’aider à créer un monde dans lequel tous les intervenants dans les domaines de la recherche, de l’université et de l’innovation sont identifiés de manière unique et sont reliés à leurs contributions et à leurs affiliations, au-delà des limites des disciplines, des frontières et des époques. » Concernant les migrations de chercheurs, l’Union Européenne et les Etat-Unis restent attractifs. En France, un cinquième des chercheurs ayant obtenu leur diplôme sur le territoire, émigre, ce qui est plutôt beaucoup… une question peut se poser : est ce que la proportion de chercheurs quittant leur pays d’obtention de doctorat ne serait pas inversement proportionnelle à l’intérêt de ce pays pour sa propre recherche scientifique…?
Ce « marqueur » – le taux d’émigration des chercheurs diplômés du pays qu’ils quittent- peut, en même temps, être lié à une bonne santé d’un système éducatif et de formation.
En effet, plus les étudiants diplômés seront perçus comme bien formés plus ils auront de facilités à le quitter, attirés par des pays dont la recherche est plus dynamique (entendons par là des pays rémunérant mieux, offrant de meilleurs capacités d’accueil) que celui dans lequel ils ont obtenu leur diplôme. En définitive, cette proportion, ce marqueur peuvent en quelque sorte être liés à une distorsion entre deux capacités pour un pays : celui de former et celui de réaliser une recherche de haut niveau permettant de garder les chercheurs que ce même pays a formé.
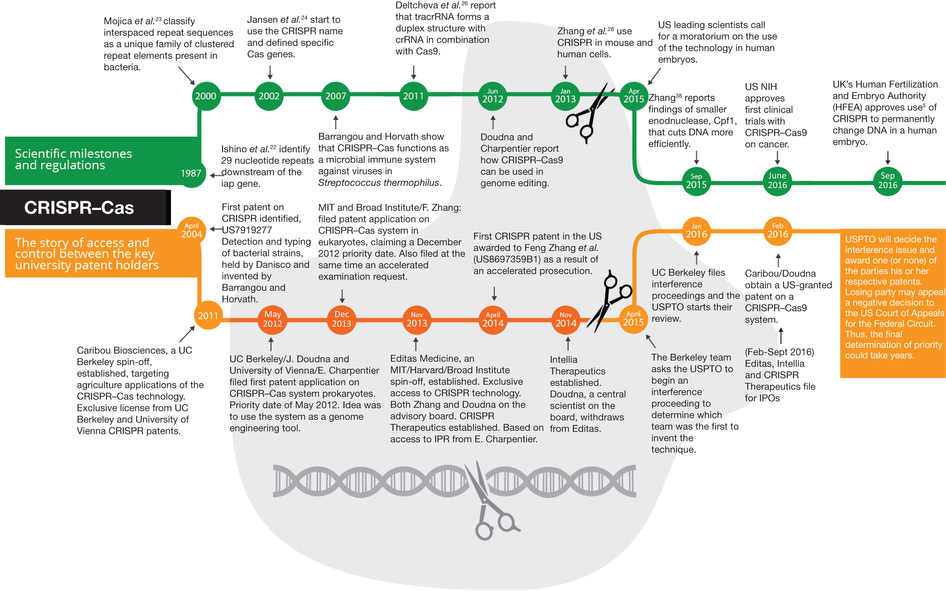
Cette figure (sur laquelle il vous faudra cliquer pour un meilleur confort de lecture) tirée de l’excellent article « The emerging patent landscape of CRISPR–Cas gene editing technology » (Nature Biotechnology – octobre 2016) vous permet d’appréhender le début de l’histoire de la technologie CRISPR/Cas9 et de vous présenter les acteurs de cette future saga de la propriété intellectuelle.
 Le développement des réseaux sociaux sur internet nous a permis d’appréhender la notion du « quand c’est gratuit, c’est toi le produit » en faisant référence, à des Facebook parmi d’autres, qui monnaient les informations personnelles des adhérents à leur service à des fins de profilage marketing. L’avènement des technologies à haut-débit en génomique a vu, il y a une dizaine d’années, émerger le concept de médecine personnalisée. Depuis, ce concept a évolué vers celui de médecine de précision (certainement plus consensuel et moins égotique). A partir de 2005, des sociétés privées se sont appropriées ce concept pour le faire déborder de la sphère de la recherche ou de la clinique pour proposer l’exploitation de profils génomiques à des fins de génomique récréative (23andMe, 2006). Un retour à l’égotisme en quelque sorte.
Le développement des réseaux sociaux sur internet nous a permis d’appréhender la notion du « quand c’est gratuit, c’est toi le produit » en faisant référence, à des Facebook parmi d’autres, qui monnaient les informations personnelles des adhérents à leur service à des fins de profilage marketing. L’avènement des technologies à haut-débit en génomique a vu, il y a une dizaine d’années, émerger le concept de médecine personnalisée. Depuis, ce concept a évolué vers celui de médecine de précision (certainement plus consensuel et moins égotique). A partir de 2005, des sociétés privées se sont appropriées ce concept pour le faire déborder de la sphère de la recherche ou de la clinique pour proposer l’exploitation de profils génomiques à des fins de génomique récréative (23andMe, 2006). Un retour à l’égotisme en quelque sorte.
23andMe a d’ailleurs un business model assez osé, consistant à vendre à des clients, leurs profils génomiques (données de puce à ADN) en échange de quelques indications concernant leur « pedigree génomique » (lire: 23 chromosomes, la NSA et moi) et quelques informations hautement critiquables. Ces dernières consistaient en des probabilités de susceptibilité à certaines afflictions (ce point là a suscité l’émoi de la FDA et ce service est aujourd’hui interrompu). En clair, 23andMe subventionne sa population de référence, ses bases de données génomiques par ses propres clients. En substance ceci constitue une évolution par rapport à Facebook, si l’on était taquin on pourrait abréger ceci en un : « vous payez pour devenir un produit ». Aujourd’hui, 23andMe habille le tout d’un « On average, a customer who consents to research contributes to over 230 studies« , se faire génotyper pour le bien de la recherche… pas loin de la servitude volontaire nappée de bon sentiment. Il est temps ici de rappeler ce que disait il y a peu un des plus grands promoteurs de la génomique personnelle : « Si je devais conseiller un jeune Craig Venter, je dirais, réfléchissez bien avant que vous veniez déverser votre génome sur Internet« . De l’aveu même de Craig Venter donc, il ne faudrait pas s’emballer avant d’envisager hypothéquer 50 % du patrimoine de ses propres enfants nés ou à naître sans qu’eux-mêmes n’aient eu mots à dire.
Aujourd’hui, arrive sur ce marché en pleine croissance, un nouvel acteur, Genos Research (page d’accueil ci-dessus). Ce dernier propose un nouveau business model : vous financez à raison de 399 USD votre propre séquençage d’exome (délivrant en moyenne 50 x fois plus de mutations que celles génotypées par l’intermédiaire des puces Illumina, telles que l’utilise 23andMe). Vous devenez propriétaire de vos données, à l’inverse des solutions concurrentes pour lesquelles, en général, vous en déléguez la propriété et l’utilisation future. Vous devenez donc le promoteur de votre propre information génomique que vous pouvez monnayer sur le marché de la recherche -priez pour avoir une maladie rare, ceci devrait accroître votre la cote de cette information. En outre, Genos permet aux utilisateurs de partager leurs données à travers leur plate-forme, ou d’exporter leurs données séquencées afin qu’ils puissent les transmettre à d’autres systèmes analytiques ou des conseillers génétiques –un business entier est d’ailleurs à bâtir : analyste de données personnelles génomiques. Genos est une société qui a bourgeonné à partir de Complete Genomics, une société de service de séquençage haut-débit, et a complété un financement privé soutenu par des entreprises en mai 2016. La société a  été co-fondée par Mark Blumling (l’ancien fondateur d’Hyperion Therapeutics, rachetée en mai 2015 par Horizon Pharma plc) et Clifford Reid (l’ancien fondateur et PDG de Complete Genomics, devenu une société de l’incroyable BGI’s company).
été co-fondée par Mark Blumling (l’ancien fondateur d’Hyperion Therapeutics, rachetée en mai 2015 par Horizon Pharma plc) et Clifford Reid (l’ancien fondateur et PDG de Complete Genomics, devenu une société de l’incroyable BGI’s company).
Pour le moins sensibles, que deviennent vos données génomiques au gré des acquisitions, fusions de sociétés de biotechnologie ? Ces changements de propriétaire sont monnaie courante et peuvent vous faire perdre de vue vos données qui pourraient finir par être le nouveau pétrole de l’ère post Donald Trump.
.jpg) Une femme américaine devient « biologiquement » plus jeune après le suivi d’une thérapie génique que sa propre société a développé. Où quand Dorian Gray fait du commerce sans nuance (attention ! jeu de mots) en mode transhumanisme 2.0.
Une femme américaine devient « biologiquement » plus jeune après le suivi d’une thérapie génique que sa propre société a développé. Où quand Dorian Gray fait du commerce sans nuance (attention ! jeu de mots) en mode transhumanisme 2.0.
Elizabeth Parrish, directrice générale de Bioviva USA Inc., est devenue, à grand renfort de communication, le premier être humain « à rajeunir » grâce à la thérapie génique développée par cette même entreprise. Cette dernière, sur la page d’accueil de son site internet, promet de démocratiser, dans un avenir proche, la thérapie génique et cellulaire. Dans un environnement convivial et confortable, les médecins de la société sont là pour corriger, avec précision, votre patrimoine corporel en voie de décrépitude.
L’un des premiers développements de la société, trouve une application dans la lutte contre le vieillissement, ce qui constitue toujours un excellent business plan compte tenu d’une corrélation établie entre âge et solvabilité. Ce philtre de jeunesse cible les télomères dont la taille serait proportionnelle à notre délai de péremption. De par leur structure particulière, les télomères requièrent d’être maintenus par une transcriptase inverse cellulaire spécifique appelée télomérase. En absence ou dans le cas de défaillance de télomérase, les télomères raccourcissent progressivement, jusqu’à atteindre une taille critique qui entraîne un arrêt des divisions cellulaires caractérisant la sénescence réplicative. Ainsi, les télomères forment une structure essentielle dans le contrôle de la viabilité cellulaire. Ceux-ci permettent de maintenir l’équilibre entre le vieillissement cellulaire et le risque de prolifération cellulaire incontrôlée.
Le score des télomères est calculé en fonction de la longueur des télomères des lymphocytes T. Ce résultat est basé sur la moyenne des longueurs des télomères des lymphocytes T par rapport à celle de la population américaine de même classe d’âge. Plus le score est élevé plus les cellules concernées seront considérées comme « jeunes » et par extension, plus le patient sera lui-même considéré comme biologiquement jeune. En septembre 2015, Elizabeth Parrish âgée de 44 ans (un peu jeune notre candidate au rajeunissement) a reçu deux des thérapies géniques expérimentales de sa propre entreprise:
- l’une pour la protéger contre la perte de la masse musculaire liée à l’âge
- l’autre combattant cette diminution quantitative de cellules souches associée au vieillissement et à ses conséquences
Le test évoqué ici a été initialement conçu pour démontrer l’innocuité de la dernière génération des thérapies géniques et cellulaires. Si les premières données s’avèrent exactes et incontestables, il s’avère que ce test constituera une première mondiale: l’allongement des télomères dont le rognage était perçu comme inéluctable, irréversible. Dans le viseur de Bioviva, le vieillissement réversible est donc en ligne de mire ou du moins les gérascophobes que le test aura rassuré voire convaincu.
Auparavant, la thérapie génique a été utilisée pour allonger les télomères des cellules murines cultivées, mais jamais sur un patient humain. En septembre 2015, les scores des télomères des globules blancs d’Elizabeth Parrish ont été collectés, par une clinique spécialisée au niveau des tests de laboratoire (SpectraCell à Houston), immédiatement avant que les traitements ne lui furent administrés. Ces scores ont révélé que les télomères d’Elizabeth Parrish étaient inhabituellement courts pour son âge, la laissant précocement vulnérable aux maladies liées à l’âge. En mars 2016, les mêmes tests ont été effectués par SpectraCell. Ces derniers ont révélé que ses télomères avaient « allongé » d’environ 20 ans, passant de 6,71kb à 7,33kb: les globules blancs d’Elizabeth Parrish sont devenus biologiquement plus jeunes. Ces résultats ont été contrôlés de façon indépendante par les fondations: Bruxelles Heales (Healthy Company Life Extension), et la fondation britannique Biogerontology Research Foundation.

Elizabeth Parrish mais qui aimerait bien le devenir
Elizabeth Parrish argumente: « actuellement, peu de thérapies offrent de réels avantages pour les personnes souffrant de maladies du vieillissement. La modification du mode de vie a un impact que limité pour le traitement de ces maladies. Les progrès de la biotechnologie apparaît être une meilleure solution, [avec ce test] nous avons fait l’histoire! ». Plusieurs signaux alimentent le scepticisme des membres de la communauté scientifique. Ainsi le fait qu’il n’y ait pas aujourd’hui de corrélation établie entre la longueur des télomères et la santé d’une personne. « C’est comme pour les cheveux gris, ce n’est pas parce qu’on se les teint qu’on vivra plus longtemps » commente Dana Glei, chercheuse à l’Université de Georgetown. Bioviva continuera de contrôler le sang de Parrish pendant les années à venir. Il reste à évaluer si le succès observé sur des leucocytes peut être étendu à d’autres tissus ou organes, est ce que ce teindre les cheveux ou rallonger ses télomères nous permet de perdre (ou gagner, cela dépend du point de vue) quelques années. Toutes ces interrogations pourraient avoir leurs réponses dans les cellules d’Elizabeth Parrish, le «patient zéro» de la thérapie génique réparatrice. Depuis ses premières injections de thérapie géniques, Bioviva a suscité un intérêt mondial, le scepticisme de communauté scientifique, l’engouement des investisseurs et à fourni un cas d’école pour tout bon bioéthicien.
Malgré, le tirage d’oreilles de la FDA (la Food and Drug Administration), les consommateurs de génomique récréative ne se sont pas réellement détournés de 23andMe, société dans laquelle Google a injecté 4,0 millions d’USD. La société de Anne Wojcicki l’ex-épouse du cofondateur de Google, Sergey Brin, n’a pas vu une perte significative de clientèle et, au contraire, a continué de recruter de nouveaux clients… pour franchir le cap du 1.000.000 durant l’année 2016.

L’implication de Google dans la société s’essoufflant (un divorce prononcé entre les fondateurs respectifs des deux sociétés, en 2015), 23andMe a cherché à transformer sa base de données de profils génomiques en profits financiers directs. Ainsi, plus d’une dizaine de sociétés ont négocié un accès à ces informations (Genentech, Pfizer, etc.). Ces informations semblent aujourd’hui constituer le vrai « business model » de 23andMe.
Si cette monétisation était complètement prévisible, il faut avouer que l’impact ou plutôt le non impact de la prise de position de la FDA atténue grandement ce que l’on avait pu annoncer au sein de l’article : 23andMe au point mort.

 A moitié scientifique et à moitié homme d’affaire, Craig Venter qui n’a pas très bon goût concernant les couvertures de ses livres essaie de mettre la main sur les données de plusieurs centaines de milliers à plusieurs millions de génomes (séquences totales ou profils génétiques). Mais que l’on se rassure c’est pour le bien de l’humanité ou au moins de la transhumanité !
A moitié scientifique et à moitié homme d’affaire, Craig Venter qui n’a pas très bon goût concernant les couvertures de ses livres essaie de mettre la main sur les données de plusieurs centaines de milliers à plusieurs millions de génomes (séquences totales ou profils génétiques). Mais que l’on se rassure c’est pour le bien de l’humanité ou au moins de la transhumanité !
Depuis 2005, les technologies de séquençage n’ont cessé d’être plus rapides et moins chères. En 2014, plus de 225.000 génomes humains étaient déjà séquencés grâce à plusieurs initiatives dont le fameux « 100 000 Genomes Project » britannique lancé en 2013. Début 2014 Illumina lançait une campagne de publicité mettant en scène le HiSeqX Ten, le premier séquenceur permettant d’atteindre la promesse d’un coût de séquençage humain à 1000 $. Cette année AstraZeneca annonçait sa collaboration avec le Human Longevity Institute de Craig Venter permettant à ce dernier un accès aux génomes ou profils génomiques de 2 000 000 de personnes d’ici 2020. En utilisant la seule séquence d’ADN, Venter dit que son entreprise peut maintenant prédire la taille, le poids, la couleur des yeux et la couleur des cheveux d’une personne, et produire une image approximative de son visage. Une grande partie de ces « détails » est dissimulé dans les variations rares, dit Venter, dont le propre génome a été mis à disposition dans les bases de données publiques depuis plus d’une décennie. Soit dit en passant, même ce promoteur d’un certain transhumanisme regrette son geste : « Si je devais conseiller un jeune Craig Venter », je dirais, réfléchissez bien avant que vous veniez déverser votre génome sur Internet« …
Quelques questions centrales demeurent et l’une d’elle consiste à envisager que le génome d’une personne n’est pas du ressort de sa seule propriété… en effet, rendre disponible son génome revient à rendre disponible une partie des informations de ces enfants et des enfants de ceux-ci etc. Effectivement, les promoteurs de la génomique à large échelle envisagent de dépasser les problématique de l’héritabilité cachée (à ce sujet, lire l’excellent article de Bertrand Jordan dans M/S : Le déclin de l’empire des GWAS). Voici un extrait très pertinent qui explicite ce problème : « Les identifications réalisées dans le cadre des études GWAS sont certes scientifiquement valables et utiles pour la compréhension du mécanisme pathogène (donc porteuses d’espoirs thérapeutiques), mais, rendant compte de moins d’un dixième des héritabilités constatées, elles passent visiblement à côté d’un phénomène important… Comment résoudre ce paradoxe ? Il faut pour cela revenir sur ce qu’examinent réellement les GWAS. Elles se limitent aux Snip, faisant (pour le moment du moins) l’impasse sur les copy number variations (CNV), ces délétions, duplications ou inversions dont on a découvert récemment plusieurs centaines de milliers dans notre génome. Et même pour les Snip, elles ne donnent pas une image complète des variations génétiques entre individus. Par la force des choses, les 500 000 Snip représentés sur les puces d’Affymetrix ou d’Illumina (et qui ont préalablement été étudiés par le consortium HapMap) correspondent à des poymorphismes assez facilement repérables dans un échantillon de population : la règle adoptée a été de ne retenir que les Snip pour lesquels la fréquence de l’allèle mineur est au moins égale à 5 %. Cet usage était nécessaire pour limiter les difficultés dans le positionnement des Snip lors de l’établissement des cartes d’haplotypes ; mais il a pour conséquences que les GWAS n’examinent que les variants fréquents… Selon une hypothèse largement répandue, les maladies multigéniques fréquentes (diabète, hypertension, schizophrénie…) seraient dues à la conjonction de plusieurs allèles eux aussi fréquents : c’est la règle « common disease, common variant » souvent évoquée depuis une dizaine d’années. Les résultats de la centaine d’études d’association pangénomiques pratiquées à ce jour indiquent que cette hypothèse est très probablement fausse : les variants communs ne rendant compte que d’une faible partie de l’héritabilité, le reste est vraisemblablement dû à des variants rares (ponctuels ou non) dont ces études ne tiennent pas compte puisque les puces utilisées ne les voient pas. »
Ainsi, pour franchir ce cap, une solution simple est envisagée : le changement de résolution avec pour credo le passage de profils génomiques (quelques millions de SNPs) à l’intégralité du génome… et après l’épigénome et en même temps le métagénome. Si ces sciences bâties sur une technologie en pleine révolution permettent l’accès à un patrimoine humain universel (l’information génomique quasi exhaustive), si ces sciences renouvellent sans cesse leurs promesses -il faut des fonds et donc convaincre les pouvoirs publics pour acheter la technologie américaine qui permet d’accomplir ces sciences- hypothéquer le patrimoine humain ou pire le privatiser pourrait être une erreur dramatique dont on a du mal à mesurer l’étendue des conséquences.
 Une jeune start-up est née en mai 2012 : cette société issue du CNRS est porteuse d’une innovation dans le secteur du séquençage haut-débit. Enfin, une alternative française aux anglosaxons qui sont présents sur le marché depuis une dizaine d’année ! Maintenant… espérons que ce nouveau né n’arrive pas trop tard sur un marché animé par des fournisseurs de séquenceurs de 2ème génération (un marché mature) et d’autres fournissant des solutions de 3ème génération, riches de promesses.
Une jeune start-up est née en mai 2012 : cette société issue du CNRS est porteuse d’une innovation dans le secteur du séquençage haut-débit. Enfin, une alternative française aux anglosaxons qui sont présents sur le marché depuis une dizaine d’année ! Maintenant… espérons que ce nouveau né n’arrive pas trop tard sur un marché animé par des fournisseurs de séquenceurs de 2ème génération (un marché mature) et d’autres fournissant des solutions de 3ème génération, riches de promesses.
PicoSeq derrière ce nom emprunt d’humilité se cache une technologie de séquençage des plus ingénieuses : en effet, SIMDEQ™ (SIngle-molecule Magnetic DEtection and Quantification) la technologie de PicoSeq utilise une approche biophysique pour extraire des informations à partir de la séquence d’ADN ou d’ARN.
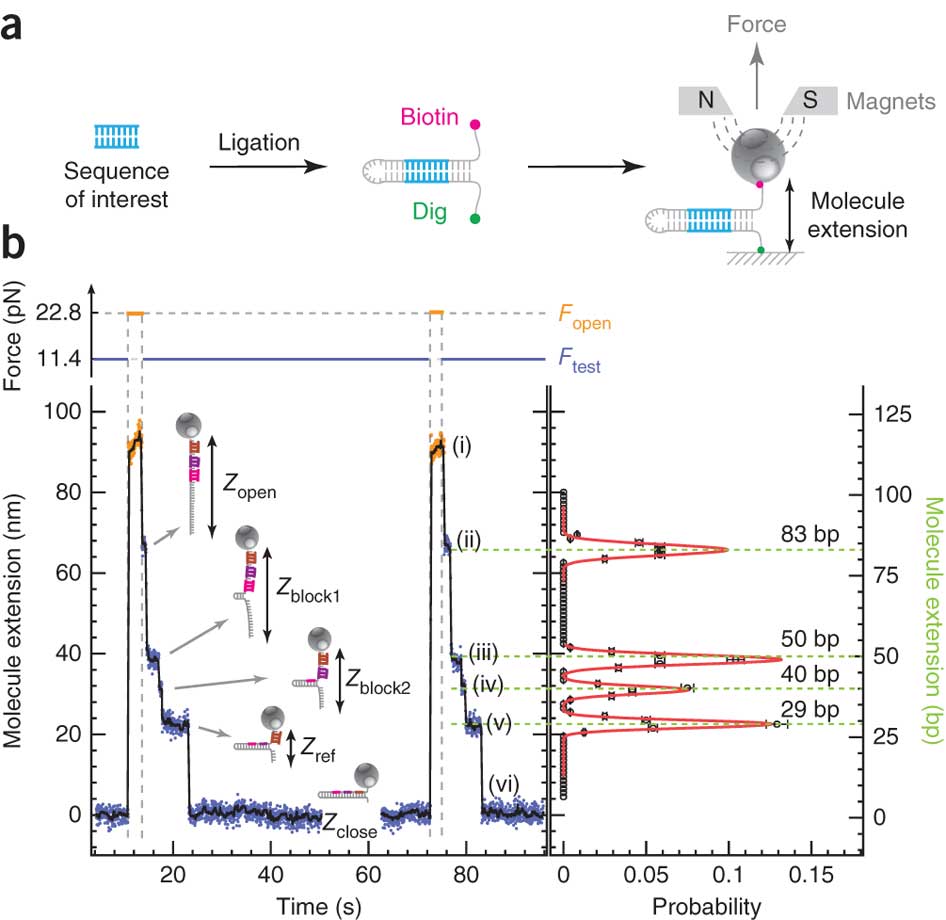
En s’appuyant sur cette représentation schématique tirée de Ding et al. (Nature Methods, 2012), on y voit un peu plus clair. Des fragments d’ADN ou d’ARN que l’on souhaite analyser servent de matrice pour la réalisation d’une librairie en «épingle à cheveux». Pour chaque épingle à cheveux, un côté d’un brin d’acide nucléique est attaché sur une surface solide plane et l’autre à une bille magnétique. En plaçant les billes dans un champ magnétique, modulant celui-ci de manière cyclique, les épingles à cheveux peuvent être auto-hybridées ou non (zip ou unzip). Ce processus peut être effectué des milliers de fois sans endommager les molécules constitutives de la librairie. La position de chaque bille est suivie à très haute précision permettant de voir ce processus d’ouverture et de fermeture en temps réel: nous avons donc là un signal brut permettant, en fonction de la force appliquée pour ouvrir totalement l’épingle à cheveu et des séquences d’oligonucléotides séquentiellement introduites dans le système de modifier la distance bille-support et de jouer sur le temps nécessaire où la force s’applique pour ouvrir l’épingle à cheveu…
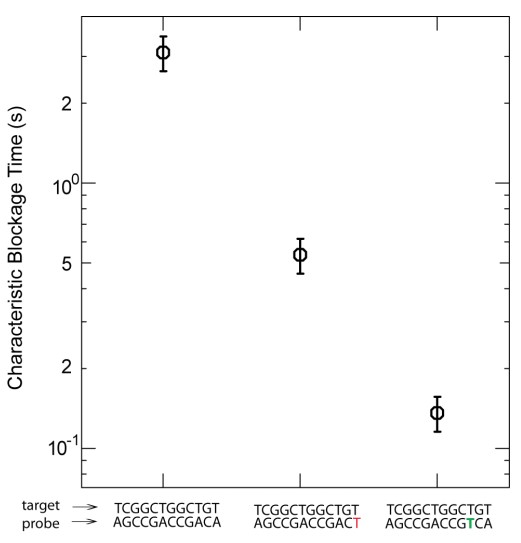
La figure ci-dessus (présente dans les données supplémentaires de l’article sus-cité) permet d’appréhender le potentiel de discrimination de la méthode… où le temps de blocage est fonction du nombre de mésappariements et de la position de ces mésappariements…
Finalement si l’aspect technique est intéressant puisqu’en rupture avec les méthodes proposées par PacBio certainement un peu moins avec le système proposé par Oxford Nanopore Technologies, si la perspective annoncée par PicoSeq est réellement séduisante: l’accès modifications épigénétiques de l’ADN, la question centrale est de savoir si le pas de la commercialisation (dans des conditions propices au succès) d’un tel outil, sera franchi.
Un article d’ Atlantico de septembre 2015, titré : les trois raisons pour lesquelles la France est incapable de rivaliser avec les géants américains de l’analyse ADN, est assez éclairant pour imaginer comment la concrétisation d’une preuve de concept peut être un chemin ubuescokafkaïen. Pour illustrer cela les propos de Gordon Hamilton, le directeur de la startup PicoSeq qui s’inquiète sur les entraves « typically french » peuvent faire office de témoignage. Ce dernier s’inquiète : « La qualité de la recherche scientifique (en France) est incroyable, l’une des meilleures » « le seul souci, c’est que l’on a beaucoup de difficultés ici à transformer ces recherches en vrai business » pour finir par citer en exemple les lenteurs administratives spécificités latines : « nous avons mis presque deux ans pour négocier les licences nécessaires aux brevets de Picoseq. Le même processus en Californie prend entre deux semaines et deux mois. Sur un marché aussi rapide que celui-ci, deux ans c’est très long. Tout change vite, c’est donc impossible pour nous d’être de sérieux concurrents de ces sociétés américaines qui ont toujours un temps d’avance ».
 Oxford Nanopore Technologies (ONT) crée un nouveau marché pour le séquençage haut-débit: le séquençage (haut-débit ?) à la portée de tous et en mode tout-terrain… mais pourquoi faire ? Le principe de cette technologie a été abordé dans plusieurs de nos articles : les données produites sont constituées de longs reads (quelques milliers de bases frôlant les 10 kB de moyenne), des reads assez bruités au-delà de 10 % d’erreurs; suffisamment longs pour permettre une identification quasi-certaine mais encore trop bruité (et trop peu profond dans le format portable MinION et maintenant SmidgION) pour pratiquer un bel assemblage de novo.
Oxford Nanopore Technologies (ONT) crée un nouveau marché pour le séquençage haut-débit: le séquençage (haut-débit ?) à la portée de tous et en mode tout-terrain… mais pourquoi faire ? Le principe de cette technologie a été abordé dans plusieurs de nos articles : les données produites sont constituées de longs reads (quelques milliers de bases frôlant les 10 kB de moyenne), des reads assez bruités au-delà de 10 % d’erreurs; suffisamment longs pour permettre une identification quasi-certaine mais encore trop bruité (et trop peu profond dans le format portable MinION et maintenant SmidgION) pour pratiquer un bel assemblage de novo.
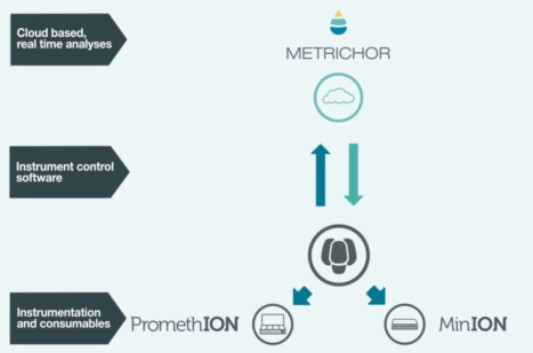
Donc imaginez vous, perdu au fin fond de l’Amazonie à la recherche de cette plante évoquée par le « sorcier » de la tribu Mashco-Piro que vous venez de quitter, plante potentiellement inconnue de notre médecine occidentale… Qu’à cela ne tienne! vous marchez en quête de la dite plante, vous, votre panneau solaire, votre smartphone, vos appareils ONT (Voltrax + SmidgION). Quasi certain de vérifier in situ votre trouvaille à l’aide d’un séquençage de 3ème génération. Enfin, ceci serait parfait si l’on oublie que Metrichor (le BaseCaller d’ONT) fonctionne en ligne… (cf schéma ci-dessous)… malgré les rêves les plus fous de Google et autres Facebook le fin fond de l’Amazonie n’est pas couvert par la 4G ! On peut imaginer qu’une application pour nos téléphones intelligents devra accompagner la mise sur le marché de cette suite d’appareils pour permettre une analyse en mode stand alone.
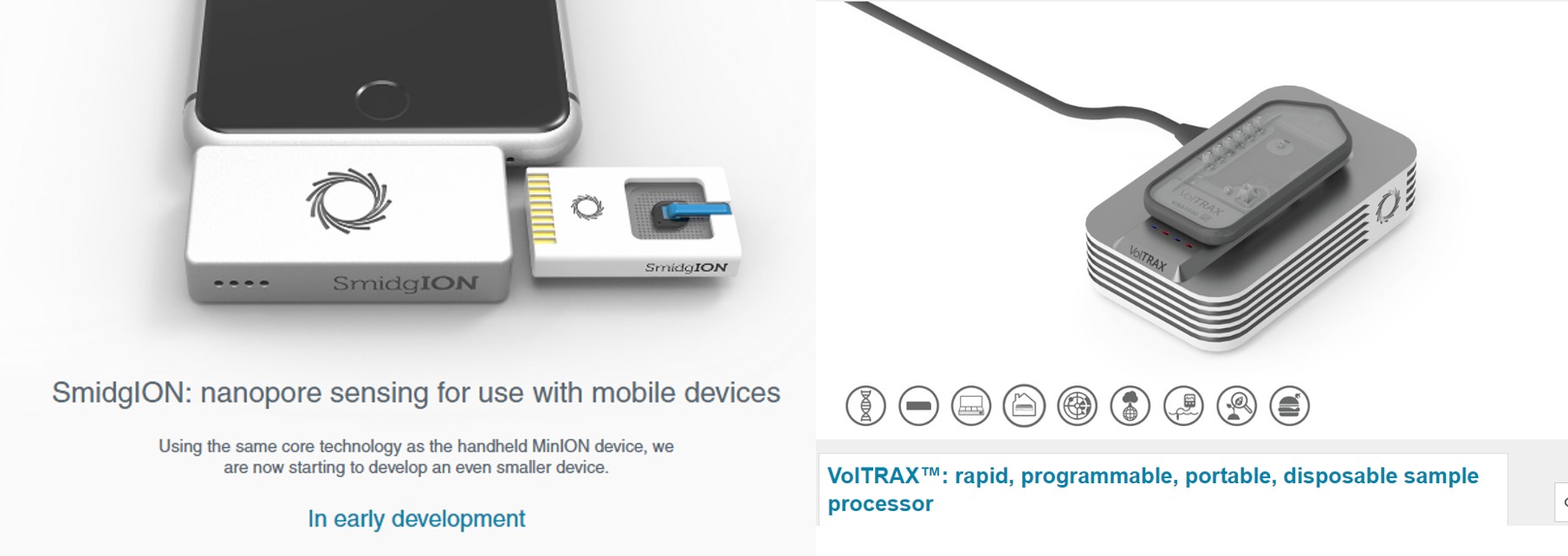
VolTRAX, l’une des promesses d’ONT, permet d’envisager la préparation de librairies à séquencer, ceci même perdu en pleine brousse. Par exemple, les nouveaux kits développés permettent une préparation d’une librairie en une dizaine de minutes. Que vous deviez séquencer un isolat du virus Zika ou Ebola sur le terrain (la logistique et le temps sont comptés) ou que vous deviez séquencer dans votre laboratoire favori, ce type d’automates permettant de simplifier les opérations relatives à l’élaboration de librairies de séquençage est souvent bien accueillis par les techniciens qui pourront s’adonner à des activités plus pertinentes.
En ce début d’année, cet article est l’occasion d’aborder rapidement les divers axes de développements, les différents acteurs du séquençage haut-débit de deuxième génération.
– Commençons par Life Technologies et sa gamme Ion Torrent. En fin d’année 2013, la Ion Community (forum où se retrouvent les utilisateurs de la technologie Ion Torrent) s’agite à l’annonce de 3 nouveautés majeures (early access program) :
(i) L’accès à une nouvelle chimie de séquençage, la Hi-Q ™, permettant d’accroître la fiabilité de séquençage. Les erreurs seraient réduites de 90 %, ceci même au niveau des homopolymères, et pour des reads de 400 bases, témoignage de Dag Harmsen à l’appui ! En clair, il semble que ce soit l’enzyme (what else ?) qui ait été remplacé.
(ii) La deuxième annonce concerne l’arrivée de la chimie Avalanche où plusieurs heures d’amplification clonale à l’aide d’un automate One-Touch peuvent être remplacées par l’emploi d’un tube, ce qui prend alors 2 heures pour obtenir une librairie de 500 pb, et ce, de façon isothermique. Un choc de simplification qui ravira les utilisateurs pour lesquels cette étape est limitante.
(iii) La troisième annonce concerne la mise à disposition de kits permettant de réaliser des analyses métagénomiques ciblées 16 S. Un système exploitant le PGM et sa capacité de produire des reads de 400 pb. L’inconnu ici réside dans la mise à disposition de la communauté d’un pipeline analytique performant.
– Qiagen, qui n’est pas connu pour être un acteur de poids sur la scène du séquençage haut-débit, arrive en force en cette année 2014 avec une solution intégrant tous les jalons nécessaires à la complétude d’une étude. Fort de son rachat d’une solution de séquençage (lire l’article : Qiagen investit… le séquençage haut-débit de 2ème génération), Qiagen propose un environnement logiciel des plus intéressants ! En effet, la société néerlandaise a racheté les sociétés CLC Bio et Ingenuity systems. Ces deux sociétés proposent l’une des toutes meilleures solutions d’analyse de séquences: une solution d’assemblage de novo réellement performante grâce à CLC genomics workbench, et Ingenuity systems proposant les pipelines d’analyses suivants: IPA, pour donner un sens biologique aux données omiques, Ireport pour l’analyse de données d’expression et Variant Analysis, un pipeline permettant d’optimiser la recherche de mutations causales.
Ainsi QIAGEN, à l’instar de ce que nous avons tâché de représenter par le schéma ci-dessous, possède actuellement tous les maillons (ou pas loin) d’une chaîne allant de l’échantillon à l’analyse finale traduisant des données de séquences en sens biologique.

– Illumina, quant à elle, semble avoir l’ambition de devenir une sorte de Apple de la « génomicosphère ». En effet, Illumina propose BaseSpace, un Itunes pour les biologistes. D’ailleurs, notons qu’Illumina propose sur Itunes une application : MyGenome, qui propose « d’explorer un véritable génome humain » et d’afficher des rapports sur les variations génétiques importantes. « L’application MyGenome fournit une interface simple, intuitive, et éducative pour vous lancer à la découverte du génome humain« . Revenons à BaseSpace, une interface entre vous et un cloud hébergeant des applications et des données permettant d’analyser les séquences en sortie de MiSeq ou HiSeq. Ce cloud permet aux utilisateurs de délocaliser le stockage de leurs données. L’idée : simplifier au maximum l’analyse par la mise à disposition d’outils et la mise en réseau des utilisateurs. Illumina s’est aperçu que si le goulot d’étranglement constitué par l’analyse de données de séquençage haut-débit volait en éclat, nécessairement les runs pourraient se multiplier avec leur chiffre d’affaire. Le schéma ci-dessous reprend quelques éléments de la solution analytique développée par Illumina.
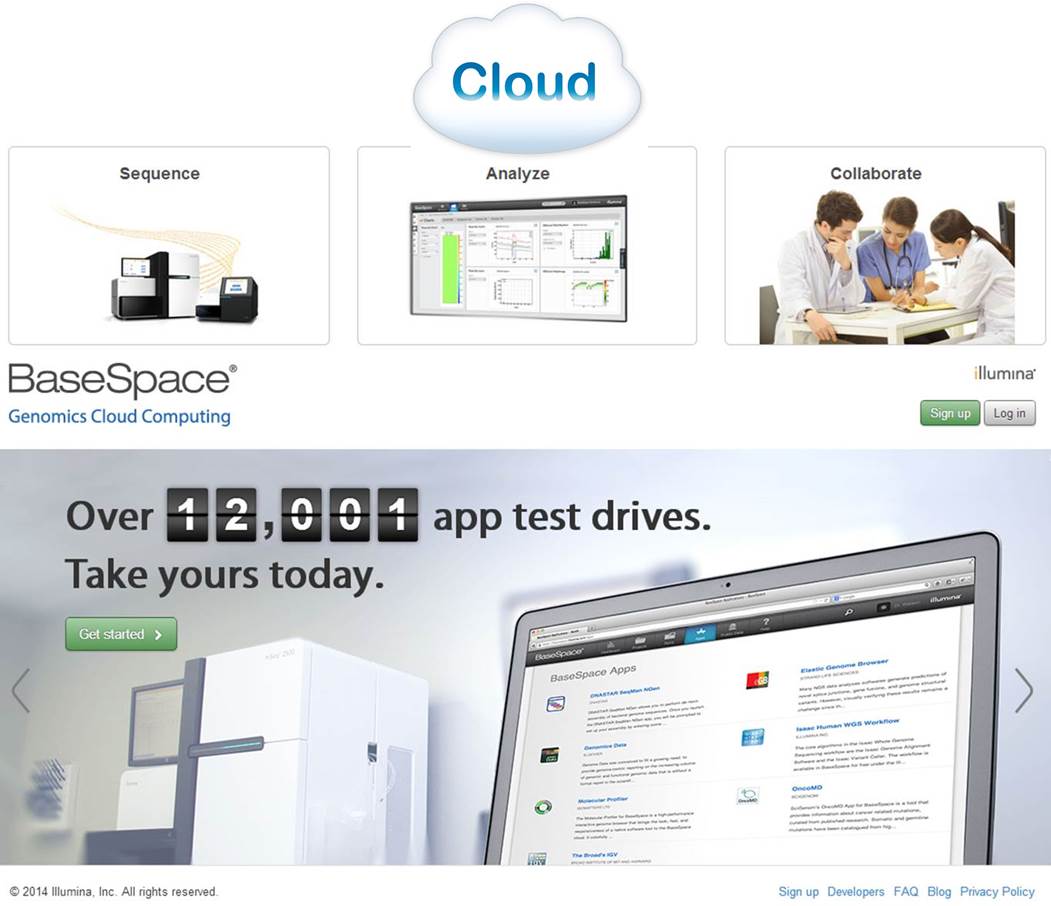
Une communauté de plus de 12000 utilisateurs, un espace permettant l’utilisation d’une vingtaine d’applications. L’objectif d’Illumina : créer un espace attractif, émulant et incitant les intervenants à mettre à disposition les applications développées en priorité sur cet espace. Anticipant une demande exponentielle d’analyses et d’espace de stockage lorsque le HiSeq a été intégré au BaseSpace, Illumina a décidé de mettre en place une politique de tarification qui limiterait la quantité d’espace libre pour stocker et traiter les données génomiques dans le cloud. En vertu de cette logique, les utilisateurs reçoivent un téraoctet gratuit d’espace pour le stockage et le traitement des données et seraient alors en mesure d’acheter du stockage supplémentaire par incréments de téraoctet ou 10 téraoctets – un téraoctet coûterait 250 $ par mois ou $ 2,000 d’avance pour une année complète , tandis que 10 téraoctets seraient à 1500 $ par mois ou une avance des frais annuels de $ 12 000 (données chiffrées début 2013).
En conclusion, si les années précédentes ont vu le lancement de nouveaux séquenceurs, avec depuis 2011 l’arrivée de séquenceurs de paillasse, les années 2013-2014 attendent la diffusion de séquenceurs de 3ème génération. Qiagen est un petit nouveau dans la course, ce nouvel acteur est capable, sans réel développement, de proposer une solution complète grâce à une stratégie de rachat pertinente. Illumina et Life Technologies, pendant ce temps, poursuivent leur développement en essayant d’émuler les utilisateurs avec, respectivement, leur BaseSpace et Ion Community. L’opérateur historique, Roche est le grand silencieux avec une stratégie peu lisible…
 La toute puissante FDA (Food and Drug Administration) a calmé les ardeurs la société 23andMe en remettant en question la diffusion par la société californienne de tests génomiques personnels. (Étonnamment ?), la FDA ne semble pas réellement heurtée par le principe même d’une société de droit privé glanant des informations génomiques pour réaliser un commerce des plus lucratifs, motus concernant le devenir de ce type de données. En réalité, l’administration américaine, soucieuse du service rendu au consommateur, émet des doutes quant à la pertinence, quant à l’exploitation des résultats, après génotypages, des individus consentants, ainsi que sur la façon dont le tout est présenté au consommateur. Ainsi, 23andMe est mise en cause au niveau de la qualité de son service. Voici son seul « crime » aux yeux de la FDA!
La toute puissante FDA (Food and Drug Administration) a calmé les ardeurs la société 23andMe en remettant en question la diffusion par la société californienne de tests génomiques personnels. (Étonnamment ?), la FDA ne semble pas réellement heurtée par le principe même d’une société de droit privé glanant des informations génomiques pour réaliser un commerce des plus lucratifs, motus concernant le devenir de ce type de données. En réalité, l’administration américaine, soucieuse du service rendu au consommateur, émet des doutes quant à la pertinence, quant à l’exploitation des résultats, après génotypages, des individus consentants, ainsi que sur la façon dont le tout est présenté au consommateur. Ainsi, 23andMe est mise en cause au niveau de la qualité de son service. Voici son seul « crime » aux yeux de la FDA!
L’administration américaine lui reproche :
– malgré les sollicitations récurrentes de la part de la FDA, 23andMe n’a pas fait valider par l’administration ses dispositifs diagnostiques in vitro. Elle n’a cessé d’allonger la liste (stratégie commerciale du restaurant chinois) des maladies et caractères que leur système était susceptible de diagnostiquer -avant « sa mise en demeure », 23andMe proposait un menu comportant le « diagnostic » de 254 prédispositions à des « maladies » ou aptitudes diverses.
– au sujet des maladies multi-factorielles, telles que le cancer de l’ovaire ou du sein, les résultats rendus aux clients sont très probablement constitués d’un grand nombre de faux positifs et de faux négatifs.
la FDA souhaite que l’intégralité des assertions de 23andMe soit validée pour que la société continue de vendre son kit phare : health-related genetic tests.
La société qui comptait régner en maître sur le marché de la génomique récréative, a peut-être fini de jouer les apprentis sorciers (franchement peu probable !). En effet, si l’intérêt de certains de ces tests génomiques, en soi, n’est pas à remettre en question, leur encadrement législatif est à souhaiter. En outre, avant de valider des kits « diagnostiques », il serait appréciable de lever le quiproquo : les kits proposés par 23andMe sont ils des dispositifs de génomique récréative ou des dispositifs médicaux ? La libéralisation incontrôlée de ce type de marchés pourrait avoir des conséquences dramatiques… Si des prédispositions peuvent être inscrites dans notre code génétique, il n’en demeure pas moins qu’une large majorité de maladies peut être qualifiée de multifactorielle.
Se sentir à l’abri d’une maladie parce que 23andMe vous rend un résultat dans ce sens ou dans le cas contraire, sentir l’ombre de l’épée de Damoclès, peut avoir, pour le consommateur de ces tests, des conséquences graves.
La lettre d’avertissement du 22 novembre 2013, de la FDA adressée à Anne Wojciki, montre l’étendue de l’ambiguïté : LETTRE d’AVERTISSEMENT ainsi que la réponse de 23andMe.
Anne Wojcicki a déclaré que « 23andMe travaille activement avec la FDA pour s’assurer que la firme fournit des informations de haute qualité afin que les consommateurs puissent avoir confiance ».
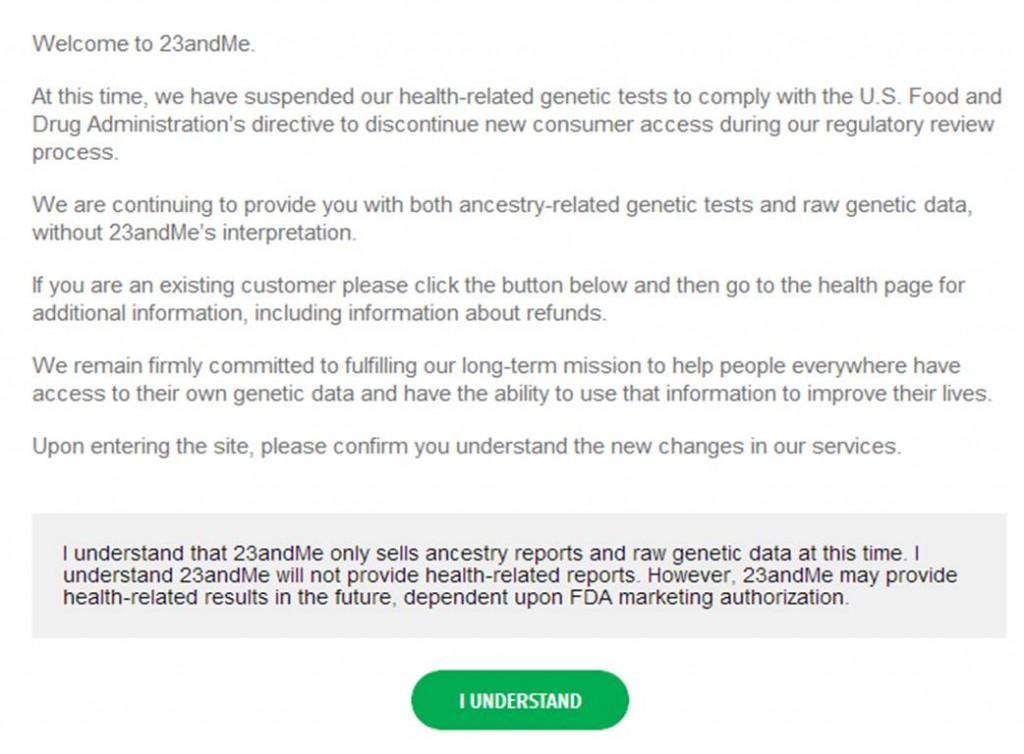
Ci-dessous, voici la nouvelle page qui vous accueille sur le site de 23andMe qui peut continuer à vendre ses tests phylogénétiques.
Comme le disait Stephen Hawking :
« J’ai remarqué que même les gens qui affirment que tout est prédestiné et que nous ne pouvons rien y changer regardent avant de traverser la rue. » (Trous noirs et bébés univers, Éditions Odile Jacob, 1994)
Qui sommes nous?
Christophe Audebert [@]
 En charge de la plateforme génomique
du département recherche et développement
de la société Gènes Diffusion .
En charge de la plateforme génomique
du département recherche et développement
de la société Gènes Diffusion .
Renaud Blervaque [@]
 Biologiste moléculaire, chargé d'études génomiques.
Biologiste moléculaire, chargé d'études génomiques.
Gaël Even [@]
 Responsable bioinformatique au sein
du département recherche et développement de la société Gènes Diffusion.
Responsable bioinformatique au sein
du département recherche et développement de la société Gènes Diffusion.
Catégories
- Analyse de données (14)
- Automatisation (5)
- Bioinformatique (27)
- Biologie (56)
- biologie transverse (35)
- Biotechnologie (30)
- Chronique littéraire (8)
- Comparatif (6)
- Diagnostic (8)
- Economie (17)
- Epidemiologie (2)
- Evénement (17)
- Formation (3)
- Gestion de projet (5)
- Grille de calcul (1)
- Intégration (5)
- Logiciels (8)
- Médecine (14)
- politique de la recherche (17)
- Recherche (21)
- Séquençage (70)
- Séquenceur (39)
- Uncategorized (25)
- Workflow (4)
Accès rapide aux articles
- Covid-19 : zoom sur les vaccins
- Comment l’ADN pourrait être le stockage de données du futur
- COVID-19 : la data visualisation au service de la science
- COVID-19 : des explications et un point d’étape au 20 février 2020
- Pour mettre du vin dans son eau
- Des petits trous, toujours des petits trous…
- Qui serait candidat ?
- Un robot pour analyser vos données…
- Monde de dingue(s)
- L’art et la manière de développer une qPCR
- Un MOOC Coursera sur le WGS bactérien
- Chercheurs & enseignants-chercheurs, l’art du multitâche.
- Un jeu de données métagénomiques
- Facteur d’impact
- Microbiote & smart city : juxtaposition de tendances
Accès mensuels
- février 2021 (1)
- décembre 2020 (1)
- février 2020 (2)
- septembre 2019 (1)
- avril 2018 (2)
- décembre 2017 (1)
- novembre 2017 (2)
- juillet 2017 (2)
- juin 2017 (5)
- mai 2017 (4)
- avril 2017 (3)
- mars 2017 (1)
- janvier 2017 (2)
- décembre 2016 (3)
- novembre 2016 (4)
- octobre 2016 (2)
- septembre 2016 (2)
- août 2016 (3)
- juillet 2016 (2)
- juin 2016 (4)
- mai 2016 (3)
- mars 2016 (1)
- novembre 2015 (2)
- avril 2015 (1)
- novembre 2014 (1)
- septembre 2014 (1)
- juillet 2014 (1)
- juin 2014 (1)
- mai 2014 (1)
- avril 2014 (1)
- mars 2014 (1)
- février 2014 (3)
- janvier 2014 (1)
- décembre 2013 (5)
- novembre 2013 (2)
- octobre 2013 (2)
- septembre 2013 (1)
- juillet 2013 (2)
- juin 2013 (2)
- mai 2013 (4)
- avril 2013 (2)
- mars 2013 (1)
- février 2013 (3)
- janvier 2013 (2)
- décembre 2012 (2)
- novembre 2012 (2)
- octobre 2012 (2)
- septembre 2012 (2)
- août 2012 (1)
- juillet 2012 (3)
- juin 2012 (5)
- mai 2012 (5)
- avril 2012 (6)
- mars 2012 (6)
- février 2012 (8)
- janvier 2012 (6)
- décembre 2011 (5)
- novembre 2011 (6)
- octobre 2011 (6)
- septembre 2011 (7)
- août 2011 (5)
- juillet 2011 (8)
Pages